Этанол
| Этанол | |
 | |
 | |
 | |
| Дөйөм үҙенсәлектәре | |
|---|---|
| Систематик исеме | Этанол |
| Ғәҙәти исеме | Этил спирты |
| Химик формула | С2H5OH |
| Рациональ формула | СH3СH2OH |
| Физик үҙенсәлектәре | |
| Агрегат хәле (Стандарт шарттарҙа) | жидкость |
| Сағыштармаса молекуляр масса | 46.069 а. е. м. |
| Моляр масса | 46.069 г/моль |
| Тығыҙлығы | 0.7893 г/см³ |
| Поверхностное натяжение | 22,39×10−3 Н/м при 20 °C Н/м |
| Термик үҙенсәлектәре | |
| Иреү температураһы | -114.3 °C |
| Ҡайныу температураһы | 78.4 °C |
| Ҡабыныу температураһы | 13 °C |
| Ялҡынланыу үҙ температураһы | 363 °C |
| Пределы взрываемости | 3,28 — 18,95 % |
| Тройная точка | -114.3 °C, ? Па |
| Критик нөктә | 241 °C, 63 бар |
| Моляр йылы һыйҙыралышлылыҡ (Стандарт шарттарҙа) | 1.197 Дж/(моль·К) |
| Энтальпия образования (Стандарт шарттарҙа) | −234,8 кДж/моль |
| Химические свойства | |
| pKa | 15.9 |
| Растворимость в һыуҙа | сикләнмәгән г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1.3611 |
| Структура | |
| Дипольный момент | (газ) 1,69 Д |
| Классификация | |
| Рег. номер CAS | [64-17-5] |
| SMILES | CCO |
| Хәүефһеҙлеге | |
| ЛД50 | 10 300 мг/кг |
| Ағыулылығы | метаболит, малотоксичен |
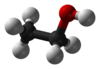
Этано́л (эти́л спирты, метилкарбино́л, шарап спирт йәки алкого́ль, ябай һөйләү телендә «спирт») — формулой C2H5OH бер атомлы спирт (эмпирик формулаһы C2H6O), башҡа варианты: CH3-CH2-OH, бер атлмлы спирттәрҙең гомологик рәтендә икенсе вәкил, нормаль шарттарҙв осоусан, яныусан, төҫһөҙ, үтә күренмәле шыйыҡса.
Алкоголле эсемлектәрҙең тәьҫир итеүсе компоненты, кешенең үҙәк нерв системаһына акыр тәьҫир итеүсе психоактив матдә, депрессант.
Этил спирты яғыулыҡ, иретеүсе булараҡ һәм спирт термометрҙарында ҡулланыла.
Алыу[үҙгәртергә | сығанаҡты үҙгәртеү]
Этил спиртын ауыуҙың ике ысулы бар — микробиологик (спиртлы әсеү) һәм синтетик (этилен гидратацияһы):
Әсеү[үҙгәртергә | сығанаҡты үҙгәртеү]
Составында углевод булған органик продукттарҙың (йөҙөм, емеше) сүпрә һәм бактерия ферменттары тәьҫире ярҙамында спиртлы әсәү элек-электән билдәле булған. Крахмал, картуф, дөгө, кукурузда шулай уҡ эшкәртелә, яғыулыҡ спирты алыу өсөн шәкәр ҡамышы һәм башҡалар эшкәртелә. Реакция бик ҡатмарлы, схемаһын түбәндәге тигеҙләмә менән бирергә була:
- C6H12O6 → 2C2H5OH + 2CO2.
Әсегән иретмәлә этонол 15%-тан артмай, сөнки ҡуйыртылған иремәлә сүпрә йәшәргә яраһыҙ. Был ысул менән алынған этанолды таҙартырға һәм ҡуйыртырға кәрәк, ғәҙәттә дистилляция ысулы менән.
Биологик сеймалдан сәнәғәттә спирт алыу[үҙгәртергә | сығанаҡты үҙгәртеү]
Аҙыү сеймалынан хәҙерге заман этил спиртын алыу технологияһы түбәндәге стадияларҙан тора:
- Крахмаллы сеймалды әҙерләү һәм ваҡлау — иген (иң беренсе — арыш, бойҙай), картуф, кукруз.и т. п.
- Ферментация. Был стадияла крахмал әсей торған шәкәргә тиклем ферментлы тарҡатыла. Для этих целей применяются рекомбинантные препараты альфа-амилазы, полученные биоинженерным путём — глюкамилаза, амилосубтилин.
- Әсеү. Сүпрә ярҙамында шәкәрҙе әсетеү нәтижәһендә әстмәлә спирт йыйыла.
- Ректификация. Ҡыуыу аппараттарында үткәрелә.
Гидролиз етештереүе[үҙгәртергә | сығанаҡты үҙгәртеү]
В промышленных масштабах этиловый спирт получают из сырья, содержащего Сәнәғәт масштабында целлюлоза (үҙағас, һалам) булған сеймалды гидролиз юлы менән алалар. Барлыҡҡа килгән пентоз һәм гексоз ҡатнашмаһын спиртҡа тиклем әсетәләр. В странах Западной Европы и Америки эта технология не получила распространения, но в СССР (ныне в России) существовала развитая промышленность кормовых гидролизных дрожжей и гидролизного этанола.
Этилен гидратацияһы[үҙгәртергә | сығанаҡты үҙгәртеү]
Сәнәғәттә, беренсе ысул менән бер рәттән, этилен гидротацияһын ҡулланалар. Гидратацияны ике юл менән үткәрергә була.
- 300 °C температурала, 300 °C баҫым аҫтында туры гидратация, активлаштырылған күмер йәки асбестҡа һөртөлгән ортофосфор кислотаһы катализатор булып хеҙмет итә:
- CH2=CH2 + H2O → C2H5OH.
- гидратация через стадию промежуточного эфира серной кислоты, с последующим его гидролизом
аралаш стадиялағы көкөрт кислотаһы эфирын артабан гидратациялау (80—90 °С ткмпературала һәм 80—90 °С баҫымда):
- CH2=CH2 + H2SO4 → CH3-CH2-OSO2OH (этилкөкөрт кислотаһы).
- CH3-CH2-OSO2OH + H2O → C2H5OH + H2SO4.
Диэтил эфиры барлыҡҡа килеүе реакцияны ҡатмарлаштыра.
Үҙенсәлектәре[үҙгәртергә | сығанаҡты үҙгәртеү]
Физик үҙенсәлектәре[үҙгәртергә | сығанаҡты үҙгәртеү]
Тышҡы күренеше: ғәҙәти шарттарҙа төҫһөҙ осоусан шайыҡса. Этил спирты һыуҙан еңелерәк. Башҡа органик матдәләрҙе яҡши иретеүсе.
| [1]: | |
| Молекуляр массаһы | 46,069 а. е. м. |
| Эреү температураһы | −114,15 °C |
| Ҡайныу температураһы | 78,39 °C |
| Критик нөктә | 241 °C (6,3 МПа баҫымында) |
| Иреүсенлек | бензол һыу, глицерином, диэтилланған эфир, ацетон, метанол, һеркә кислотаһы, хлороформ менән бутала. |
| Показатель преломления | 1,3611(температурный коэффициент показателя преломления 4,0·10−4,справедлив в интервале температур 10—30 °C) |
| Стандартная энтальпия образования ΔH | −234,8 кДж/моль (г) (при 298 К) |
| Стандартная энтропия образования S | 281,38 Дж/моль·K (г) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 1,197 Дж/моль·K (г) (при 298 К) |
| Энтальпия плавления ΔHпл | 4,81 кДж/моль |
| Энтальпия кипения ΔHкип | 839,3 кДж/моль |
95,57 % этанол + 4,43 % һыу ҡушылмаһы азеотроп ҡушылма булып тора, т. е. әммә ҡыуған ваҡытта айырыла.
Химик үҙенсәлектәре[үҙгәртергә | сығанаҡты үҙгәртеү]

Һелтеле металдар менән тәьҫир итешә, этилат һәм водород барлыҡҡа килә.
- 2C2H5OH + 2К = 2С2Н5ОК + Н2.
Карбон кислоталары менән ҡатмарлы эфирҙар барлыҡҡа килтерә:
- RCOOH + HOCH2CH3 → RCOOCH2CH3 + H2O
Көкөрт кислотаһы булғанда (120 °C түбенерәк температурала) дегидратация реакцияһына керә, деэтил эфиры барлыҡҡа килә:
- 2 CH3CH2OH → CH3CH2OCH2CH3 + H2O
120 °C юғары температурала көкөрт кислотаһы булғанда тулылармаған углеводородтар барлыҡҡа килтерә:
- CH3CH2OH → CH2CH2 + H2O
Кислород булған һауала йылы булеп сығарып яна:
- C2H5OH + 3 O2 → 2 CO2 + 3 H2O
Һелтеле металдар һәм уларҙын гидраттары менән тәьҫир итәшә, этилатар барлыҡҡа килә.
- 2 CH3CH2OH + 2 Na → 2 CH3CH2ONa + H2
- CH3CH2OH + NaH → CH3CH2ONa + H2
Цинк хлориды булғанда гидрогалогенирование реакцияһына инә:
- CH3CH2OH + HCl → CH3CH2Cl + H2O
Ҡулланыу[үҙгәртергә | сығанаҡты үҙгәртеү]
Яғыулыҡ[үҙгәртергә | сығанаҡты үҙгәртеү]
Этанол эске яныула двигательдәрҙә яғыулыҡ итеп файҙаланыла (донъяла беренсе немец «Фау-2» баллистик ракетаһында яғыулыҡ урынына этанол ҡулланылған). Спирттың классик нефть яғыулыҡтары менән ҡушылмай ҡатлауланғанға ҡулланыу сикләнгән. Юғары октанла яғыулыҡ һәм бензин компоненты булараҡ ҡулланыла.
Химия сәнәғәтендә[үҙгәртергә | сығанаҡты үҙгәртеү]
- ацетальдегид, диэтил эфиры, тетраэтилсвинец, уксус кислотаһы, хлороформ, этилацетат, этилен һ.б. химик мтдәләр алыу өсөн сеймал булп хеҙмәт итә;;
- лак-буяу сәнәғәтендә иреткес итеп, көнкүреш химияһы тауарҙары етештереүҙә һәм башҡа өлкәләрҙә;
- антифриз һәм тәҙрә йыуыусы шыйыҡсалар компоненты;
- көнкүрештә этанол быяла һәм сантехника йыһаздарын таҙартыу өсөн файҙаланыла. Является растворителем для репеллентов.
Медицина[үҙгәртергә | сығанаҡты үҙгәртеү]

- тәьҫире буйынса этил спиртын антисептиктар рәтенә ҡуйырға була;
- как обеззараживающее и подсушивающее средство, наружно;
йоғошһоҙландырыу һәм киптереү сараһы,
- 96%-лы этил спиртының киптереүсе һәм дублаусы үҙенсәлеге оперция урынын һәм ҡайһы бер методикаларҙа хирургтың ҡулып эшкәртеү өсөн ҡулланыла;
- дарыуҙарҙы иреткес, үҫемлек сеймалынан төнәтмә һәм экстракт һ.б. әҙерләү өсөн;
- төнәтмә һәм экстракттарҙы консервациялау өсөн (минималь концентрация 18 %);
- үпкәләрҙе яһалма һулыш алдырғанда күбекте баҫыу өсөн;
- йылытыусы компрестарҙа;
- биҙгәк тотҡанда һыуытыу өсөн (ыуыныу өсөн)[2];
- медикаменттар булмағанда дөйөм анестезия өсөн;
- как пеногаситель при отеке легких в виде ингаляции 33 % раствора;
- метонол, этиленгиколь кеүек ағыулы спиртар менән ағыуланғанда ағыу ҡайтарғыс булараҡ файҙаланыла.
Парфюмерия һәм косметика[үҙгәртергә | сығанаҡты үҙгәртеү]
Төрлө матделәрҙе иреткес булараҡ хушбуй, одеколон, аэрозолдар составына инә һәм төп компоненты булып тора. Теш пастаһы, шампуньдар һ.б. составында ҡулланыла.
Аҙыҡ сәнәғәте[үҙгәртергә | сығанаҡты үҙгәртеү]
Һыу менән бер рәттән спиртлы эсемлектәрҙең төп компоненты (араҡы, виски, джин, һыра һ.б.) Әсеү юлы менән алынған һайһы бер эсемлектәрҙә, әммә алкогольһыҙ һаналған эсемлектәрҙә бар (кефир,кеүәҫ, ҡумыҙ, алкогольһыҙ һыра һ.б.). Кефирҙа этанол бик әҙ кимәлдә (0,12 %), йылы урында оҙаҡ торған кефирҙа 1 % булыуы мөмкин. Ҡумыҙҙа 1—3 % этанол (әсеһендә 4,5 %), кеүәҫтә — 0,5 -тән 1,2 %-ҡа тиклем[3].
Аҙыҡ ароматизаторҙары иреткесе. Икмәк-күмәс өсөн консервант һәм кондитер сәнәғәтендә ҡулланыла.[4]
Аҙыҡ-түлеккә өҫтәмә булараҡ теркәлгән E1510[5].
Этанолдың энергия ҡиммәте — 7,1 ккал/г.
Башҡалары[үҙгәртергә | сығанаҡты үҙгәртеү]
Биологик препатараттарҙы консерациялау өсөн ҡулланыла.
Донъяла этанол етештереү[үҙгәртергә | сығанаҡты үҙгәртеү]
Илдәр буйынса этанол етештереү, млн литр. ethanolrfa.org мәғлүмәте.
| 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010est | |
| АҠШ | 13 362 | 16 117 | 19 946 | 24 565 | 34 776 | 40 068 | 45 360[6] |
| Бразилия | 15 078 | 15 978 | 16 977 | 18 972,58 | 24 464,9 | ||
| Евросоюз | - | - | - | 2 155,73 | 2 773 | ||
| Китай | 1 837,08 | 1 897,18 | |||||
| Индия | 199,58 | 249,48 | |||||
| Франция | - | - | |||||
| Германия | - | - | |||||
| Рәсәй | 609 | 536 | 517 | 700 | |||
| ЮАР | - | - | |||||
| Великобритания | - | - | |||||
| Испания | - | - | |||||
| Таиланд | 299,37 | 339,4 | |||||
| Колумбия | 283,12 | 299,37 | |||||
| Бөтә донъя : | 40 710 | 45 927 | 50 989 | 49 524,42[7] | 65 527,05 |
Иҫкәрмәләр[үҙгәртергә | сығанаҡты үҙгәртеү]
- ↑ Этиловый спирт: химические и физические свойства
- ↑ Средства, влияющие на ЦНС 2007 йыл 3 июль архивланған.
- ↑ [1] Федеральное агентство по техническому регулированию и метрологии. ГОСТ Р 52409-2005 (полный текст)
- ↑ Russell, Nicholas J. Food preservatives. — New York: Kluwer Academic/Plenum Publishers, 2003. — P. 198. — ISBN 0-306-47736-X.
- ↑ E1510 — спирт этиловый
- ↑ 2008 Ethanol Production Exceeds 9 Billion Gallons
- ↑ Ethanol World Production Statistics 2009 йыл 24 март архивланған.
Һылтанмалар[үҙгәртергә | сығанаҡты үҙгәртеү]
| Этанол Викимилектә |
