Аҡһымдар
| Аҡһымдар | |
 | |
| Ҡайҙа өйрәнелә | protein science[d] һәм химия белков[d] |
|---|---|
| Кодирующий ген | белок-кодирующий ген[d] |
| Модель элементы | протеин[d] |
| EntitySchema для класса | Ошибка Lua в Модуль:Wikidata на строке 301: Неизвестный тип сущности.. |
Аҡһымдар — аминокислоталар ҡалдығынан торған юғары молекуляр органик берләшмәләр[1]. Тере матдәнең даими һәм иң мөһим өлөшө булып, төҙөлөш һәм функция нигеҙен тәшкил итәләр.
Пептид бәйләнеш ярҙамында сылбырға теҙелгән альфа-аминокислоталарҙан торған юғары молекулалы органик матдәләр.
Дөйөм мәғлүмәттәр
[үҙгәртергә | сығанаҡты үҙгәртеү]Күҙәнәктең органик матдәләренән һаны һәм әһәмиәте буйынса аҡһымдар беренсе урында тора.
Бөтә аҡһымдарҙың составына ла водород, кислород, азот атомдары инә. Күп кенә аҡһымдарҙың составына, былагрҙан тыш, көкөрт атомдары инә (С — 54 %, О — 23 %, Н — 7 %, N — 17 %, S — 2 %). Шулай уҡ составына металл атомдары — тимер, цинк, баҡыр, магний, марганец, фосфор атомдары ингән аҡһымдар бар.
Башҡа органик берләшмәләрҙән айырмалы рәүештә, аҡһымдарҙың күп кенә үҙенсәлектәре бар. Иң элек аҡһымдарға ғәйәт ҙур молекуляр масса хас.
Этил спиртының молекуляр массаһы—46, һеркә кислотаһының—60, бензолдың—78, глюкозаның — 180 булһа, альбуминдың (йомортҡа аҡһымдарының береһе) —36000, гемоглобиндың (ҡыҙыл ҡан күҙәнәктәренең аҡһымы) —152000, миозиндың (мускул-дарҙағы аҡһымдарҙың береһе)—500 000 тирәһен тәшкил итә.
Башҡалар менән сағыштырғанда аҡһым молекулалары ифрат ҙур. Уларҙың төҙөлөшөндә меңәрләгән атом ҡатнаша (Һөт аҡһымы- казеиндың формулаһы: C1894H3021O576N468S21)
Бындай молекулаларҙың ҙурлығын күрһәтеү өсөн уларҙы макромолекула (гр. «макрос» — ҙур, гигант) тип атайҙар.
Органик берләшмәләр араһында аҡһымдар иң ҡатмарлыһы. Улар полимерҙар тип аталған берләшмәләргә ҡарай. Полимер молекулаһын мономер тип аталған сағыштырмаса ярайһы уҡ ябай структураның күп тапҡыр ҡабатланған оҙон сынйыры тәшкил итә. Әгәр мономерҙы А хәрефе менән билдәләһәк, полимерҙың структураһын ошолай күрһәтергә булыр ине: А—А—А—А—А.
Тәбиғәттә аҡһымдарҙан тыш башҡа күп полимерҙар бар, мәҫәлән, ңеллюлоза, крахмал, каучук. Химия промышленносында күп яһалма полимерҙар барлыҡҡа килтерелгән (полиэтилен, лавсан, капрон һәм башҡалар). Тәбиғи һәм яһалма полимерҙарҙың күбеһе бер төрлө мономерҙарҙан төҙөлгән.
Аҡһымдарҙың мономерҙары оҡшаш, әммә улай уҡ бер төрлө түгел.
Аҡһымдың мономерҙары булып ά-аминокислоталар тора. Аминокислотаның молекулаһы ике өлөштән тора. Бер өлөшө бөтә аминокислоталарҙа ла бер төрлө.
Был функциональ төркөмсәләр: карбоксил төркөмө — СООН (кислота үҙсәнлектәрен бирә) һәм аминотөркөм — NH2 (нигеҙ үҙсәнлектәрен бирә).
Аминокислоталар бер-береһенән молекулаһының икенсе өлөшө — радикал буйынса айырыла.
Күп төрлө аминокислоталарҙың булыуы билдәле. Әммә һәр тәбиғи аҡһым мономеры сифатында — хайуандар, үҫемлектәр, микробтар, вирустарҙа — тик 20 ά-аминокислота булыуы билдәле. Улар «тылсымлы» тигән исем алған.
Бөтә организм аҡһымдарының бер үк аминокислоталарҙан төҙөлгән булыуы — Ерҙәге тереклектең бер тамырҙан булыуына тағы бер дәлил.
Аҡһым молекулаһын барлыҡҡа килтергәндә аминокислоталарҙың бер-береһенә тоташыуы бөтә аминокислоталар өсөн дә дөйөм булған төркөмсәләр аша башҡарыла.
Химик реакция барышында бер аминокислотаның карбоксил төркөмө күрше аминокислотаның амин төркөмө менән бәйләнешкә инә. Һөҙөмтәлә,һыу молекулаһы айырылып сыға һәм бушанған валентлыҡ иҫәбенә аминокислоталарҙың ҡалған өлөштәре тоташа.
Аминокислоталар араһында пептид бәйләнеш тип аталған ныҡлы ковалент бәйләнеш -NН—СО— барлыҡҡа килә.
Аминокислоталарҙан барлыҡҡа килгән берләшмә пептид тип атала. Ике аминокислотанан яһалған пептид — дипептид, өс аминокислотанан — трипептид, күп аминокислоталарҙан яһалғаны полипептид тип атала.
Бөтә аҡһымдар полипептидтарҙы, йәғни тиҫтәләгән, хатта йөҙәрләгән аминокислоталар быуындарынан торған сынйырҙы, тәшкил итә.
һәр тере организмда күп һандағы һәр төрлө аҡһымдар була. Шул уҡ ваҡытта һәр төрҙөң үҙенә генә хас үҙенсәлекле аҡһымдары бар.
Хатта төрлө төрҙәге хайуандарҙа бер үк функцияны үтәгән аҡһымдар бер-береһенән айырыла. Мәҫәлән, бөтә умыртҡалы хайуандар: балыҡтар, амфибиялар, ҡоштар, һөтимәрҙәр ҡанының ҡыҙыл күҙәнәктәрендә бөтә хайуандарҙа бер үк функцияны үтәүсе — кислород йөрөтөүсе аҡһым гемоглобины бар.
Әммә һәр хайуан төрөнөң гемоглобины үҙенсә, структураһы һәм үҙсәнлектәре буйынса башҡа хайуандарҙың гемоглобинынан айырылып тора.
Аҡһымдарҙың күп төрлөлөгө
[үҙгәртергә | сығанаҡты үҙгәртеү]Аҡһымдар — пептид бәйләнеше менән сылбырға йыйылған альфа-аминокислоталарынан торған юғары молекуляр төҙөлөшлө органик матдәләр.
Тере организмдарҙа аҡһымдарҙың аминокислота составы генетик код менән билдәләнә. Синтез ваҡытында күп осраҡта 20 стандарт аминокислота ҡулланыла.
Уларҙың комбинациялары күплеге аҡһым молекулалары үҙенсәлегенең төрлөлөгөн бирә.
Аҡһымдарҙың ғәйәт күп төрлөлөгө:
- аҡһымдарҙа аминокислоталарҙың составына (нисә төр),
- аминокислоталар быуыны һанына,
- уларҙың сынйырҙа урынлашыу тәртибенә бәйләнгән.
Был осраҡта структуралар төрө астрономик һандарға етә. Мәскәүҙә биохимик конгреста һинд ғалимы Синг үҙенең докладында ошондай ҡыҙыклы иҫәпләүҙәр килтерҙе.
34 000 молекуляр массалы аҡһымдың 300-гә яҡын аминокислота быуыны бар (бер аминокислота быуынының уртаса молекуляр массаһы 110-ға тигеҙ).
Был аҡһымдың составына 20 аминокислотаның бөтәһе лә түгел, тик 12-һе генә инә, тип ҡарайыҡ. Бындай шарттарҙа ошо аҡһым өсөн мөмкин булған изомерҙар һаны 10300 -гә тигеҙ.
Бының ниндәй ҙур һан икәнен һиҙемләр өсөн, 10300 тиклем бер тинлектәрҙе күҙ алдына килтерегеҙ. Был тинлек аҡсалар өйөмө 10300 г ауырлыҡта (бер тинлек аҡса 1 г). Ер шарының массаһы 1027 г.
Аҡһымдарҙың структураһы
[үҙгәртергә | сығанаҡты үҙгәртеү]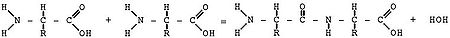
Әгәр ҙә бер аминокислота быуынының оҙонлоғо 35— 37 нм икәнен иҫәпкә алғанда, йөҙәрләгән аминокислота ҡалдыҡтарынан торған аҡһым макромолекулаһының оҙонлоғо бер нисә тиҫтә нанометр булырға тейеш.
Ысынында иһә аҡһым молекулалары күпкә бәләкәйерәк. Уларҙың ҡайһы берҙәре 5—7 нм диаметрлы шар рәүешендә. Аҡһымдың полипептид сынйыры нисектер бөгәрләнеп, уңайлап һалынған, һәр аҡһымға айырым бер төрлө итеп һалыу хас.
Полипептид сынйырҙағы эҙмә-эҙлелек һәм уның билдәле тәртиптә компакт формаға төрөлөү ысулдары аҡһым структуралары, йәки төҙөлөш кимәлдәре тип атала. Аҡһым молекулаһының төҙөлөшөн тулыһынса характерлау өсөн уның беренсел, икенсел һәм өсөнсөл структуралары тураһында белеү кәрәк.
Төҙөлөш кимәлдәре
[үҙгәртергә | сығанаҡты үҙгәртеү]
К. Линдстрём-Ланг аҡһым молекулаҙының 4 төҙөлөш кимәлен айырырға тәҡдим итә: беренсел, икенсел, өсөнсөл, дүртенсел[2].
Беренсел структура
[үҙгәртергә | сығанаҡты үҙгәртеү]Аҡһым молекулаһында аминокислоталар ҡалдыҡтарының эҙмә-эҙлеклелеге уның беренсел структураһын билдәләй.
Был, икенсе төрлө әйткәндә, аҡһымдың формулаһы. Беренсел структураны, йәки аминокислоталар ҡалдыҡтарының эҙмә-эҙлеклелеген уны кодлаусы ген һәм генетик код билдәләй. Полипептид сылбырҙа аминокислота ҡалдыҡтары үҙ-ара бик көслө поляр ковалент бәйләнеш — пептид бәйләнештәре тотоп тора.
Икенсел структура
[үҙгәртергә | сығанаҡты үҙгәртеү]Бөтәһенән йышыраҡ полипептид сынйыры тулыһынса йәки өлөшләтә спираль булып бөгәрләнә (α- структура). Был осраҡта аминокислота радикалдары спиралдең тыш яғында ҡала.
Спиралдең уратымдары тығыҙ урынлашҡан. Бер уратымдың NН-төркөмдәре менән күрше уратымда урынлашҡан СО-төркөмдәре араһында водородлы бәйләнештәр барлыҡҡа килә.
Йәки сылбыр гармун күреге кеүек бөкләнә (β- структура). Бында ла күрше күрек биттәре араһында NН-төркөмдәре менән СО-төркөмдәре барлыҡҡа килтергән водородлы бәйләнештәр урынлаша.
Водородлы бәйләнештәр ковалент бәйләнештәргә ҡарағанда күпкә көсһөҙөрәк, әммә, күп тапҡыр ҡабатланып, улар ныҡлы бәйләнеш булдыра.
Күп һанлы водородлы бәйләнештәр менән «тегелгән» полипептид спираль (α- структура) йәки күрек (β- структура) ярайһы уҡ ңыҡлы структураны тәшкил итә
Был аҡһымдың икенсел структураһы.
Өсөнсөл структура
[үҙгәртергә | сығанаҡты үҙгәртеү]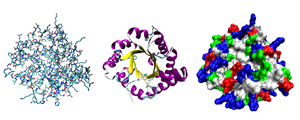
Полипептид спираль артабанғы рәтләп һалыуға дусар ителә. Ул хикмәтле рәүештә йомарлана (глобула). Әммә һәр аҡһымдың үҙенә генә хас һәм даими урыны була. һөҙөмтәлә өсөнсөл структура тип аталған конфигурация хасил була.
Өсөнсөл структураны гидрофоб аминокислоталарҙың радикалдары араһында барлыҡҡа килгән гидрофоб бәйләнештәр тотоп тора.
Был бәйләнештәр водородлы бәйләнештәргә ҡарағанда көсһөҙөрәк. Гидрофоб радикалдар һыуҙан этеләләр һәм бер-береһе менән йәбешәләр. Шулай итеп, һыу мөхите аҡһым молекулаһына билдәле бер тәртиптәге структураны ҡабул иттергән кеүек була, һәм ул биологик йәһәттән активлаша.
Өсөнсөл структура — полипептид сылбырҙың пространствола урынлашыу торошо. Өсөнсөл структураны тотоп тороусы бәйләнештәр:
-СООН и -ОН (сложноэфирный мостик) -СООН и -NH2 (солевой мостик)
- -S-S- (дисульфид күпер);
- -СООН һәм -ОН (ҡатмарлы эфир күпере);
- -СООН һәм -NH2 (водород бәйләнештәре);
- радикалдар араһындағы гидрофоб бәйләнештәр.
Дүртенсел структура
[үҙгәртергә | сығанаҡты үҙгәртеү]Дүртенсел структура (субъединица, йәки домен) — бер нисә полипептид сылбыр берләшеп төҙөгән аҡһым комплексы. Был комплексты барлыҡҡа килтереүсе полипептид сылбырҙар бер үк төрлө булырға, йәки төрлө сылбырҙар булырға ла мөмкин. Дүртенсел структураны ла өсөнсөл структураны тотоп тороусы бәйләнештәр нығытып тора.
Аҡһымдарҙың үҙсәнлектәре
[үҙгәртергә | сығанаҡты үҙгәртеү]Төрлө тере объекттарҙан — хайуандарҙан, үҫемлектәрҙән, микроорганизмдарҙан — меңәрләп төрлө аҡһым алынған һәм өйрәнелгән.
Аҡһымдарҙың физик һәм химик үҙсәнлектәренең күп төрлө булыуы хайран ҡалдыра. Был уларҙың аминокислоталар составының төрлөлөгөнән килеп сыға.
һыуҙа бөтөнләй эремәгән һәм еңел эрегән аҡһымдар бар. Химик яҡтан бик үк актив булмаған, төрлө химик агенттарҙың тәьҫиренә тотороҡло булған аҡһымдар бар.
Бик әҙ генә тәьҫир аҫтында, мәҫәлән, тоноҡ ҡына яҡтылыҡтан йәки еңелсә генә ҡағылыуҙан, үҙгәреүсән ифрат тотороҡһоҙ аҡһымдар бар.
Оҙонлоғо йөҙәр нанометрға еткән еп рәүешендәге аҡһымдар бар. 5—7 нм диаметрлы шар кеүек йомро молекулалы аҡһымдар бар.
Әммә һәр ваҡыт аҡһымдың структураһы һәм үҙсәнлектәре ҡәтғи рәүештә уларҙың башҡарған функцияһына тап килә.
Ҡорос кеүек ҡаты, тотороҡло кератин аҡһымынан хайуандарҙың һаҡланыу һәм агрессия ҡоралы — мөгөҙҙәре, тояҡтары, панцирҙары, тырнаҡтары, ҡанаттары, сәстәре яһалған.
Еп һымаҡ молекулалы аҡһымдар мускулдар составына инә. Улар ҡыҫҡарыуға һәм оҙонайыуға һәләтле һәм күҙәнәктәрҙең хәрәкәт реакцияларын тәьмин итә.
Ваҡ йомро молекулалы еңел эреүсән, хәрәкәтсән аҡһымдар матдәләрҙе күсереп йөрөтөү өсөн файҙаланыла.
Юғары активлы, еңел үҙгәреүсән структуралы аҡһымдар катализатор функцияһын үтәй, шулай уҡ тышҡы мөхиттән, күҙәнәккә сигналдарҙы ҡабул итеү һәм тапшырыу өсөн файҙаланыла.
Төрлө физик һәм химик факторҙар — юғары температура, күп кенә химик матдәләр, нурландырыу, механик баҫым яһау — тәьҫире аҫтында аҡһымдың икенсел һәм өсөнсөл (әммә беренсел түгел) структураларын тотоп тороусы көсһөҙ бәйләнештәр өҙөлә һәм молекула тарҡала.
Аҡһымдың тәбиғи структураһы боҙолоуы -денатурация тип атала. Денатурация һөҙөмтәһендә аҡһымдың үҙсәнлектәре үҙгәрә. Ул эреүсәнлеген юғалта, аш һеңдереү ферменттары эшмәкәрлегенә юл асыла, үҙенә хас булған функциялар үҙгәрә. Йомортҡа эсендәге шыйыҡлыҡтың йылытҡандан һуң тығыҙ һәм үтә күренмәүсәнгә әйләнгәнен күҙәткән һәр кешегә һис шикһеҙ денатурация күренеше таныш.
Денатурация процесы ҡайтмалы (ренатурация), йәғни йәйелгән полипептид сынйыр үҙенән-үҙе спираль булып төрөлөүгә, ә спираль — үҙенән-үҙе өсөнсөл структура яһауға һәләтле.
Был аҡһым төҙөлөшөнөң бөтә үҙенсәлектәре уның беренсел структураһы менән, йәғни полипептид сынйырҙа аминокислоталарҙың составы һәм уларҙың сиратлашып килеү тәртибе менән, билдәләнеүен аңлата.
Физик һәм химик факторҙарҙың тәьҫиренән аҡһымдарҙың структураны ҡайтмалы үҙгәртеүгә булған һәләте бөтә тере системаның иң мөһим үҙсәнлеге — ярһыусанлыҡ нигеҙендә ята.
Синтез
[үҙгәртергә | сығанаҡты үҙгәртеү]
Аҡһымдарҙы төҙөлөшө буйынса төркөмләү
[үҙгәртергә | сығанаҡты үҙгәртеү]- Фибрилляр аҡһымдар— төрлө полипептид сылбырҙар араһында бәйләнештәр барлыҡҡа килтергән структура. Фибрилляр аҡһымдар күҙәнәктәрҙең һәм туҡымаларҙың структураларын барлыҡҡа килтереүҙә ҡатнашҡан микрофиламенттарҙы, микроторбаларҙы, фибрилл ептәрҙе төҙөй. Фибрилляр аҡһымдарға кератин һәм коллаген инә.
- Глобуляр аҡһымдар —сферик формалағы һыуҙа эреүсән молекулалар.
- Мембрана аҡһымдары — күҙәнәк мембранаһын үтәнән-үтә биләп торған аҡһым комплекстары.
Йыш ҡына күҙәнәк араһына һәм цитоплазмаға сығып торған өлөштәре була.
Мембрана аҡһымдары рецептор функцияһын үтәй, сигналдар тапшыра, мембрана аша төрлө матдәләрҙе транспортлауҙа ҡатнаша.
Аҡһым-транспортёрҙар махсуслашҡан тәртиптә эшләй. Һәр береһе тик билдәле төр матдәне генә үткәрә йәки билдәле бер сигналды тапшыра.
Ябай һәм ҡатмарлы аҡһымдар
[үҙгәртергә | сығанаҡты үҙгәртеү]Ябай аҡһымдар (протеиндар): альбуминдар, глобулиндар, гистон, коллаген, кератин һәм башҡалар. Ябай аҡһымдар полипептид сылбырҙан ғына тора.
Ҡатмарлы аҡһымдарҙың (протеидтар) составында полипептид сылбырҙан тыш аҡһым булмаған компоненттар (простетик төркөм) инә.
Ҡатмарлы аҡһымдарҙың химик тәбиғәте буйынса төркөмдәре:
- нуклеопротеидтар — аҡһым һәм нуклеин кислоталарының берләшмәһе. Улар араһында иң өйрәнелгәне — рибосомалар. Улар бер нисә РНК молекулаларынан һәм рибосома аҡһымдарынан тора.
Хроматин — эукариот күҙәнәктәрҙең төп нуклеопротеиды. ДНК-нан һәм структур аҡһымдар — гистондарҙан тора (күҙәнәк ядроһында, митохондрияларҙа, хлоропластарҙа);
- гемопротеидтар — аҡһым булмаған компоненты гемдан , 4 пирроль ҡулсанан, уларға бәйләнгән (азот атомы аша) ике валентлы тимер ионынан тора.
Бындай аҡһымдарға гемоглобин, миоглобин, цитохромдар инә. Уларҙы хромопротеидтар тип тә атайҙар. Сөнки, улар гем был матдәләргә төҫ бирә.
- металлопротеидтар -простетик төркөмөндә металл булған ҡатмарлы аҡһымдар. Хлорофилл дың гемында магний, цитохром составында баҡыр бар;
- липопротеидтар — простетик төркөмө булып липидтар тора. Улар күҙәнәк мембранаһын төҙөйҙәр;
- фосфопротеидтар — простетик төркөмө булып фосфор кислотаһы ҡалдығы тора. Уларға казеин (һөттә), овальбумин һәм вителлин (йомортҡала), ҡайһы бер ферменттар инә;
- гликопротеидтар — простетик төркөмө булып углеводтар тора (мәҫәлән, шайыҡтағы муцин).
Аҡһымдарҙың функцияһы
[үҙгәртергә | сығанаҡты үҙгәртеү]Аҡһымдар күҙәнәктә күп төрлө һәм мөһим функциялар башҡара.
- Төҙөү функцияһы. Күҙәнәк мембранаһы һәм күҙәнәк органоидтары аҡһымдан тора. Юғары төҙөлөшлө хайуандарҙа ҡан тамырҙары стенкалары, тарамыштар, кимерсәктәр һ. б., нигеҙҙә, аҡһымдарҙан тора.
- Аҡһымдарҙың каталитик функцияһы. Химяя курсынан билдәле булыуынса, химик реакцияларҙың тиҙлеге реакцияға ингән матдәләрҙең үҙсәнлеге, уларҙың концентрацияһы һәм реакция барған температура менән бәйле.
Ҡағиҙә булараҡ, тере күҙәнәктәге матдәләрҙең химик активлығы ҙур түгел. Уларҙың күҙәнәктәге концентрацияһы ла күп осраҡта ҙур булмай.
Күҙәнәк мөхитенең температураһы юғары түгел. Шулай булғас, күҙәнәктәге реакциялар бик әкрен үтергә тейеш кеүек.
Әммә күҙәнәктәге реакциялар ҙур тиҙлек менән бара. Быға күҙәнәктә катализаторҙар булыу арҡаһында өлгәшелә. Күҙәнәк катализаторҙары ферменттар тип атала.
Ферменттарҙың каталитик активлығы ифрат ҙур. Улар реакцияны унар, йөҙәр миллион тапҡыр тиҙләтә.
Ферменттар химик структураһы буйынса — аҡһымдар. Күпселек осраҡта ферменттар молекулаларының ҙурлыҡтары буйынса фермент макромолекулаларына ҡарағанда бик бәләкәй булған матдәләрҙең әүерелеүҙәренә катализатор була.
Мәҫәлән, каталаза ферментының молекуляр массаһы 250 000, ә водород пероксидының (Н2О2) (уны тарҡатҡанда катализатор ролен каталаза үтәй) молекуляр мас саһы бары тик 34. Фермент һәм ул тәьҫир иткән матдәләр ҙурлыҡтарының шундай нисбәте, ферменттың каталитик активлығы уның бөтә молекулаһы менән түгел, ә ҙур булмаған өлөшө — ферменттың актив үҙәге менән билдәләнелә, тип фекерләргә нигеҙ бирә.
Билдәле булыуынса, матдәләр араһында реакңия уларҙың молекулалары бик ныҡ яҡынлашҡан осраҡта ғына бара. Ферменттың һәм матдәнең бер-береһенә яҡынлашыуына ферменттың актив үҙәге һәм матдәләр молекулаһы структураларының геометрик тура килеүе мөмкинлек тыуҙыра.
Улар бер-береһенә «асҡыс менән йоҙаҡ» кеүек тап килә. Ферменттың денатурацияһы ваҡытында уның каталитик активлығы юғала, сөнки актив үҙәктең структураһы боҙола.
Күҙәнәктәге һәр химик реакция тип әйтерлек үҙенә генә хас фермент менән катализлана. Күҙәнәктә барған төрлө реакцияларҙың һаны бер нисә меңгә етә. Шуға ярашлы күҙәнәктә лә бер нисә мең төрлө фермент барлығы билдәле.
- Сигнал функциялары. Күҙәнәктең тышҡы йөҙө мембранаһына тышҡы мөхит факторҙары тәьҫиренә яуап итеп үҙенең өсөнсөл структураһын үҙгәртеүгә һәләтле аҡһымдарҙың молекулалары теҙелгән. Тышҡы мөхиттән сигналдарҙы ҡабул итеү һәм күҙәнәккә командалар тапшырыу ошо юл менән бара.
- Хәрәкәт функцияһы. Хәрәкәт — тереклек активлығының бер күрһәткесе. Юғары төҙөлөшлө хайуандар күҙәнәктәренең бөтә төр хәрәкәткә булған һәләтен, шул иҫәптән мускулдарҙың ҡыҫҡарыуын, шулай уҡ ябай төҙөлөшлөләрҙә керпексәләрҙең елпелдәп тороуын, ҡамсылыларҙың хәрәкәтен, айырым ҡыҫҡартып тороусы аҡһымдар башҡара.
- Транспорт функцияһы. Улар, төрлө матдәләрҙе үҙенә ҡушып, күҙәнәктең бер урынынан икенсе урынына күсереп йөрөтөүгә һәләтле. Ҡандың аҡһымы гемоглобин кислородты үҙенә ҡуша һәм кәүҙәнең бөтә туҡымаларына һәм органдарына тарата.
- Аҡһымдарҙың һаҡлау функцияһы. Сит аҡһымдарҙың һәм күҙәнәктәрҙең организмға килеп эләгеүе була, шунда уҡ был ят күҙәнәктәрҙе үҙенә бәйләүсе һәм зарарһыҙландырыусы айырым аҡһымдар эшләнеп сыға башлай.
- Энергетик функция. Аҡһымдар күҙәнәктә аминокислоталарға тиклем тарҡала. Аминокислоталарҙың бер өлөшө аҡһымдар синтезлауға китә, икенсе өлөшө тулыһынса тарҡала, һәм был осраҡта энергия бүленеп сыға. 1 г аҡһым тулыһынса тарҡалғанда 17,6 кДж энергия бүленеп сыға.
Акһымдарҙың биосинтезы
[үҙгәртергә | сығанаҡты үҙгәртеү]
Төп төшөнсәләр
[үҙгәртергә | сығанаҡты үҙгәртеү]- ДНК
- Матрица реакциялары
- Репликация
- Транскрипция
- Трансляция
- Ген
- Генетик код
- Триплет
- Кодон
- антикодон
- И-РНК, йёкм мРНК
- т-РНК
- Полисома
- ФЦР
Аҡһым биосинтезының әһәмиәте
[үҙгәртергә | сығанаҡты үҙгәртеү]Күҙәнәктә бер нисә мең төрлө аҡһым бар. Шулай уҡ, күҙәнәктең һәр төрөнөң үҙенә генә хас үҙенсәлекле аҡһымдары була. Тик үҙенең генә аҡһымын синтезлау һәләте күҙәнәктән күҙәнәккә нәҫел буйынса бирелә һәм бөтә ғүмере буйы һаҡлана.
Бөтә күҙәнәктәр ҙә ғүмере буйы аҡһымдар синтезлай. Сөнки тереклек иткәндә аҡһымдар бер туҡтауһыҙ тарҡалып тора. Уларҙың структураһы һәм функцияһы боҙола. Аҡһымдарҙың бындай молекулалары яңы молекулалар менән алмаштырыла. Шуның арҡаһында күҙәнәктең тереклеге һаҡланып ҡала.
Нәҫел мәғлүмәте һәм уның күҙәнәктә тормошҡа ашыу юлы
[үҙгәртергә | сығанаҡты үҙгәртеү]Организмдар үҙҙәренең төҙөлөш һәм тереклек үҙенсәлектәрен быуындан быуынға тапшырыу һәләтлегенә эйә. Йәғни,үҙҙәренең төрөнә хас заттар хасил итеү, үрсеү һәләтлегенә эйә. Был һәләтлек нигеҙендә нәҫелсәнлек мәғлүмәте ята. Был мәғлүмәттәе йөрөтөүсе булып ДНК молекулалары тора. Бының нигеҙендә ДНК молекулаһының фундаменталь үҙсәнлектәре ята. Ул үҙсәнлектәрҙе матрица реакциялары тип атайҙар:
- Репликация — ДНК молекулаһының үҙ копияһын (күсермәһен) эшләү реакцияһы, икеләтелә алыу һәләтлеге.
- Транскрипция — ДНК молекулаһындағы мәғлүмәтте и-РНК (мәғлүмәтле РНК) молекулаһына күсереү реакцияһы.
- Трансляция — РНК молекулаһындағы мәғлүмәт нигеҙендә аҡһым молекулаһын синтезлау реакцияһы.
Тереклектең ғәжәйеп үҙенсәлектәренең береһе: уларҙың төҙөлөшөндәге һәм тереклегендәге оҡшашлыҡ һәм, шул уҡ ваҡытта, ғәйт күп төрлөлөкте булдырыусы айырмалар.
Хатта бер төр эсендә лә заттар морфологик, физиологик, биохимик үҙсәнлектәре, билдәләре буйынса айырыла. Тикшеренеүҙәр күрһәтеүенсә, оҡшашлыҡ һәм айырмалар аҡһымдар составы менән билдәләнелә.
Систематика буйынса яҡыныраҡ торған организмдарҙа оҡшаш аҡһымдар күберәк була, һәм киреһенсә.
Шул уҡ ваҡытта, систематикала бик алыҫ торған организмдарҙа ла, бер үк функция үтәгән аҡһымдар бер төрлө йәки оҡшаш төҙөлөшлө була. Мәҫәлән, эттең һәм кешенең организмында инсулиндың төҙөлөшөндә айырма бик әҙ генә.
Әммә кешенең ҡан төркөмөн билдәләүсе аҡһымдар араһында айырма бик ҙур.
Һәр организмдың үҙенсәлеге, уникаллеге нигеҙендә аҡһымдарҙың төрлөлөгө ята.
Эритроциттарҙағы (ҡандың диск формаһындағы ҡыҙыл тәнсәләре) гемоглобин (А) дүрт полипептид сынйырҙан (ике α-сынйыр һәм ике β-сынйыр) торған ҡатмарлы аҡһым булып тора. Төп функцияһы — күҙәнәктәргә кислород ташыу.
Нәҫел анемияһы (серповидная анемия) менән сирләгән кешеләрҙә эритроциттар ярым ай формаһында була.
Сәбәбе: сирле кешеләрҙә гемоглобиндың беренсел структураһы боҙола. Сир HBB генындағы мутацияға бәйләнгән:β-сынйырҙа 6-сы аминокислота − глутамин валин менән алмашына.
Был аномаль гемоглобин (S) кислородты ташыу функцияһын тейешле кимәлдә башҡара алмай. Шулай итеп, гемоглобиндағы 574 аминокислотының икә-һе генә алмашыныу ҙа, икенсел, өсөнсөл һәм дүртенсел структураһының боҙолоуына, нәҫел сиренә алып килә.
ДНК — синтезы өсөн матрица
[үҙгәртергә | сығанаҡты үҙгәртеү]- Нисек итеп сәләмәт эритроциттарҙа миллионлаған гемоглобин молекулалары бер иш, аминокислота ҡалдыҡтарының теҙмәһе бер үк төрлө була ала һуң ул?
- Нисек итеп структураһы боҙолған эритроциттарҙағы гемоглобин молекулаларында бер үк урында бер иш хата ҡабатлана һуң ул?
Был нәк китап баҫтырғандағы кеүек. Тираж эсендә нисә экземпляр китап сығарылһа ла, улар бер үк матрицанан баҫылғас бер үк төрлө була. Әгәр матрицала хата китһә, ул бөтә китаптарҙа ла ҡабатлана.
Күҙәнәктәрҙә матрица ролен ДНК молекулалары үтәй. Унда структур аҡһымдарҙың төҙөлөшө тураһында ғына түгел, ә бөтә төр (ферменттар, гормональ, сигнал һәм башҡа аҡһымдар тураһында ла мәғлүмәт ята.
ДНК коды
[үҙгәртергә | сығанаҡты үҙгәртеү]Синтезлана торған аҡһымдың структураһын билдәләүҙә ДНК төп роль уйнай.
ДНК-ның еп һымаҡ молекулаһында күҙәнәк аҡһымының беренсел структураһы тураһында мәғлүмәт һалынған. Билдәле бер аҡһымдың беренсел структураһы хаҡында мәғлүмәт биргән ДНК молекулаһының киҫеге ген тип атала. ДНК молекулаһында бер нисә йөҙ ген була.
Аҡһымдың беренсел структураһы нисек итеп ДНК-ла программаға һалынғанын аңлар өсөн Морзе азбукаһын миҫал итеп килтереп була.
Морзе азбукаһы буйынса әлифбалағы бөтә хәрефтәр, тыныш билдәләре, һандар, ҡыҫҡа (нөктә), оҙон (һыҙыҡ) сигналдарҙың комбинациялары менән билдәләнгән. Телеграф, радио аша хәбәр тапшырыу өсөн ҡулланылған шартлы тамғалар йыйылмаһы код йәки шифр тип атала. Морзе азбукаһы кодтың миҫалы булып тора.
ДНК — эҙмә-эҙ урынлашҡан нуклеотидтарҙан торған сынйыр, ә аҡһым — эҙмә-эҙ урынлашҡан аминокислоталар сынйыры.
Морзе кодында һәр хәрефкә нөктә һәм һыҙыҡтарҙың билдәле бер йыйылмаһы тура килгән кеүек, ДНК кодында ла нуклеотидтарҙың билдәле бер тәртиптә урынлашыуы аҡһым молекулаһында билдәле бер аминокислоталарҙың шуға ярашлы урынлашыуын тәьмин итә.
Аҡһымдың беренсел структураһы тураһында ДНК молекулаһында яҙылған мәғлүмәтте аңлар өсөн, ДНК-ның кодын белергә кәрәк. Йәғни нуклеотидтарҙың ниндәй йыйылмаһы ниндәй аминокислотаға тура килеүен белергә кәрәк. Нуклеотидтар бөтәһе — 4, ә аминокислоталар — 20 төр. Тимәк, һәр аминокислотаға нуклеотидтарҙың бер нисә йыйылмаһы тура килә.
Әгәр икешәр нуклеотид теҙмәһе менән кодланһа, 16 ғына йыйылма булыр ине. Шуға ла, аҡһымдың һәр аминокислотаһы ДНК сынйырында эҙмә-эҙлекле урынлашҡан өс нуклеотидтың йыйылмаһы менән кодлана: 4 элементтан өсәрләп 64 төрлө йыйылма төҙөргә була. Был бөтә 20 аминокислотаны ла кодҡа һалыр өсөн артығы менән етә.
Хәҙерге ваҡытта ДНК кодының шифрҙары тулыһынса асылған. һәр аминокислота өсөн өс нуклеотидтан торған триплеттарҙың составы аныҡ билдәләнгән.
ДНК кодында күп осраҡта бер үк аминокислота берәү генә түгел, ә бер нисә — ике, дүрт, хатта алты триплет менән кодҡа һалынған. Кодтың бындай үҙсәнлеге нәҫел информацияһын һаҡлау һәм тапшырыуҙың ышаныслылығын арттырыу өсөн әһәмиәтле тигән фекер бар.
64 триплет араһында өс — УАА, УАГ һәм УГА— аминокислоталарҙы кодҡа һалмай (терминаль, йәки стоп-кодондар). Был триплеттар— полипептид сынйыр синтезының бөтөүе тураһында сигнал.
Бындай триплеттарҙың кәрәклеге шунда: йыш ҡына и-РНК-ла бер нисә полипептид сынйыр синтезлана. Бына шуларҙы бер-береһенән айырыу өсөн күрһәтелгән триплеттар файҙаланыла ла инде.
Күҙәнәктә информация ағымы
[үҙгәртергә | сығанаҡты үҙгәртеү]Информация (мәғлүмәт) ағымы башында ДНК молекулаһы тора. Ундағы информация һөйләм һымаҡ юл менән яҙылған. Информация ағымының кульминацияһы булып аҡһым молекулаһының синтезланыуы тора. Шулай итеп, ағымы һөҙөмтәһендә ДНК молекулаһындағы информация (мәғлүмәт) аҡһым молекулаһына күсерелә.
Информация ағымы этаптары
[үҙгәртергә | сығанаҡты үҙгәртеү]- Транскрипция — комплементарлыҡ принцибы нигеҙендә ДНК молекулаһындағы мәғлүмәтте и-РНК (мәғлүмәтле РНК) молекулаһына күсереү реакцияһы.
- Трансляция — РНК молекулаһындағы мәғлүмәт нигеҙендә аҡһым молекулаһын синтезлау реакцияһы. ДНК молекулаһындағы һөйләм һымаҡ яҙылған дүрт кодлы информацияны « егерме хәрефле» аҡһым кодына күсереү. Был « егерме хәрефле» аҡһым молекулаһы һәр аҡһым төрөнең үҙенә генә хас уникаль конфигурация — өсөнсөл структура яһап төрөлә.
Транскрипция
[үҙгәртергә | сығанаҡты үҙгәртеү]
Аҡһым синтезы рибосомаларҙа бара, ә аҡһымдың структураһы тураһындағы мәғлүмәттәр ядрола урынлашҡан ДНК-ла шифрланған.
- Нисек һуң улар ядронан цитоплазмалағы рибосомаларға килә?
Информацияны тапшырыу и-РНК ярҙамында бара. Улар ДНК молекулаһының бер өлөшө — ген— сынйырҙарының береһендә синтезлана һәм уның структураһың теүәл ҡабатлай.
- Гендағы нуклеотидтарҙың эҙмә-эҙлекле урынлашыуы һәм составы нисек итеп и-РНК-ға «күсереп яҙыла» һуң?
Ике спиралле ДНК молекулаһы комплементар принцип нигеҙендә төҙөлә. Был принцип и-РНК синтезында ла үҙ көсөндә ҡала. И-РНК-синтетаза ДНК-ың ике полинуклеоитид сынйырын айыра бара, артынса ДНК сынйырҙарының береһендәге нуклеотидтарҙың һәр береһе ҡаршыһына и-РНК-ның комплементар нуклеотиды килеп баҫа.
Тик РНК-ла азот нигеҙле Т(тимин) нуклеотиды урынына азот нигеҙле У(урацил) нуклеотиды ҡатнаша. Шулай итеп, Гднк ҡаршыһына — Црнк, Црнк ҡаршыһына — Грнк, Тцнк ҡаршыһына— Арнк, Аднк ҡаршыһына Урнк килеп баҫа. һөҙөмтәлә и-РНК-ның барлыҡҡа килгән сынйыры икенсе сынйырҙың аныҡ күсермәһен тәшкил итә.
Ошо юл менән гендағы информаңия и-РНК-ға күсереп яҙыла. Был проңесс транскрипция тип атала (лат. «транскрипцио» — күсереп яҙыу).
Аҙаҡ и-РНК молекулалары фермент-транспортерҙар ярҙамында аҡһым синтезланған ергә, йәғни рибосомаларға, йүнәлә. Шунда уҡ цитоплазманан аҡһымдың төҙөлөш материалдары булған аминокислоталар үтеп инә. Күҙәнәк цитоплазмаһында һәр ваҡыт аҙыҡ аҡһымдарының тарҡалыуы һөҙөмтәһендә барлыҡҡа килгән аминокислоталар була.
Аҡһым синтезлаусы система нимәләрҙән тора
[үҙгәртергә | сығанаҡты үҙгәртеү]- Мәғлүмәтле РНК (и-РНК, йәғни мРНК) —системаның төп компоненты;
- Аҡһым мономерҙары булып торған 20 төр аминакислота;
- Аминокислоталарҙы аҡһым синтезлана торған урынға ташыусы транспорт — кәмендә 20 төр тРНК; улар и-РНК-ғы триплетлы код менән аҡһымдағы (полипептид) аминокислоталар эҙмә-эҙлелеген араһында бәйләүсе звено.
- Ферменттар — кәмендә егерме төр аминоацил-тРНК-синтетаза;ферменттың һәр төрө үҙенә тәғәйен тРНК молекулаһын һәм үҙенә генә тәғәйен аминокслотаны танырға, табырға, үҙенә бәйләргә тейеш;
- рибосомалар төркөмө (4-12 рибосоманан торған төркөм полисома тип атала, йәғни улар бергәләп бер и-РНК молекулаһында теҙелеп, бер үк төр аҡһым молекулаһын йыя)
- АТФ- һәм АМФ- әүҙемләштереүсе ферменттар системаһы
- Аҡһым синтезлауҙа ҡатнашыусы ГТФ
- Цитоплазманың әүҙемләштереү факторҙары
Транспорт РНК-һы
[үҙгәртергә | сығанаҡты үҙгәртеү]
һәр аминокислота рибосомаға махсус транспорт РНК-һы (т-РНК) оҙатыуында килеп эләгә. Тәбиғи аҡһымдарҙы төҙөүҙә 20 төрлө аминокислота ҡатнаша, тимәк, 20-нән дә кәм булмаған төрлө т-РНК бар.
Т-РНК сынйырының күп кенә урынында бер-береһенә комплементар 4—7 эҙмә-эҙлекле нуклеотид быуыны була. Был быуындарҙа комплементар нуклеотидтар араһындағы водородлы бәйләнештәр барлыҡҡа килә. һөҙөмтәлә формаһы менән клевер япрағына оҡшаған ҡатмарлы элмәкле структура барлыҡҡа килә.
Уның осонда генетик код буйынса айырым бер аминокислотаға тура килгән нуклеотидтар триплеты урынлашҡан. Ул код триплеты, йәғни антикодон тип атала. Ә «клевер япрағының» һап яғында аминокислотаны бәйләүсе быуын урынлашҡан.
Т-РНК-ның код триплетының нуклеотидтар составы и-РНК триплетының нуклеотидтар составына комплементар. Мәҫәлән, аланинлы т-РНК-ның код триплеты — ЦГА (и-РНК-ла уға ГЦУ триплеты комплементар).
Валинлы т-РНК-ның код триплеты — ЦАА (и-РНК-ла уға ГУУ триплеты комплементар. Шулай итеп, һәр т-РНК үҙенең аминокислотаһын «тейәй» һәм рибосомаға алып бара.
Рибосомала полипептид сынйырҙың синтезы
[үҙгәртергә | сығанаҡты үҙгәртеү]Матрицалы реакциялар — тере күҙәнәккә генә хас үҙенсәлек. Улар бөтә тереклектең фундаменталь үҙсәнлегенә — үҙҙәренә оҡшаштарҙы барлыҡҡа килтереү һәләтенә нигеҙ булып тора.
Нуклеотидтарҙың эҙмә-эҙлелеге рәүешендә и-РНК-ға яҙылған аҡһым структураһы тураһында информация синтезланыусы аҡһым молекулаһында аминокислоталарҙың эҙмә-эҙлекле урынлашыуын трансляция тип атайҙар (лат. «трансляцио» — күсереү).
Информацион РНК буйлап теҙелеп, бер иш аҡһым молекулаларын синтезлаусы рибосомалар йыйылмаһын полисома тип атайҙар. Беренсе рибосома и-РНК-ның еп һымаҡ молекулаһының һул яҡ осонан килеп инә һәм аҡһым синтезы башлана. Аҡһым молекулаһы йыйылыу барышында рибосома и-РНК буйлап үрмәләй.
Рибосоманың алға шыуыуы була, шул уҡ остан и-РНК-ға икенсе рибосома килеп инә, беренсеһе кеүек үк, синтезлай башлай һәм беренсе рибосома артынан алға хәрәкәт итә. Артабан и-РНК-ға өсөнсө, дүртенсе һ. б. рибосомалар килеп инә.
Улар бөтәһе лә бер үк эш башҡара: һәр береһе ошо и-РНК-ла алдан программаланған бер үк аҡһымды синтезлай. Рибосома и-РНК буйлап ни тиклем алға шыуған булһа, аҡһым молекулаһының шул тиклем ҙурыраҡ өлөшө «йыйылған» була. Рибосома и-РНК-ның икенсе осона килеп етеүгә синтез тамамлана.
Барлыҡҡа килгән аҡһым менән бергә рибосома и-РНК-нан төшөп ҡала. Артабан улар айырыла.
Рибосома яңынан теләһә ниндәй и-РНК-ға беркетелеп, теләһә ниндәй ы аҡһымды синтезларға һәләтле. Аҡһым молекулаһы эндоплазма селтәргә сыға һәм уның буйлап күҙәнәктең ошо аҡһымға мохтаж булған урынына йүнәлә.
Информацион РНК(и-РНК) молекулаһына бер үк ваҡытта һыйған рибосомалар һаны уның оҙонлоғона бәйле. Мәҫәлән, гемоглобин аҡһымы синтезын программалаған и-РНК молекулаһына биш рибосомаға тиклем һыя.
Рибосоманың эш механизмы
[үҙгәртергә | сығанаҡты үҙгәртеү]Трансляция барған рибосоманың ҙурлығы 6 нуклеотид оҙонлоғона, йәғни ике триплетҡа тигеҙ. Тимәк, рибосома и-РНК буйлап шыуғанда рибосоманың функциональ үҙәгендә (ФЦР) һәр саҡ бер үк ваҡытта нуклеотидтарҙың йәнәш 2 триплеты була.
ФЦР-ҙың функцияһы: и-РНК-ның ике триплетына антикодондары менән т-РНК-лар килеп бәйләнгән мәлдә, улар тейәгән аминокислоталарҙы үҙ-ара пептид бәйләнеш аша бәйләү.
Рибосома и-РНК буйлап бер триплеттан икенсеһенә талғын ғына түгел, ә өҙөк-өҙөк, «аҙымлап» күсә.Бер аҙымы — бер триплет. Рибосома һикереп, киләһе триплетҡа күскәндә, алдағы триплет т-РНК-һы менән ФЦР-ҙан сығып китә һәм бер-береһенән ысҡына.
Бушаған урынға комплементарлыҡ принцибына ярашлы аминокислотаһы менән яңы т-РНК килеп тора. Рибосома ҡыҫҡа ғына ваҡытҡа туҡтап ҡала.
Трансляция операцияһы 1/5—1/6 секундтан да күп ваҡыт алмай. Ә полипептид сынйыр бер быуынға оҙоная. Артабан күрше триплетҡа тағы бер «аҙым» эшләнелә һәм яңынан ҡыҫҡа ваҡытҡа туҡталыш яһала. Бына шулай и-РНК буйлап осҡа хәтлем хәрәкәт дауам итә.
Билдәле бер аҡһымдың нисә молекулаһы кәрәк булһа, шунса һанда рибосамалар биосинтез башҡарып сыға. Ихтыяжға етерлек аҡһым синтезланыу менән, был процестың төп компоненты — и-РНК һәм был аҡһымды синтезлаусы система тарҡала.
Рибосома— күҙәнәктәге аҡһым синтезының "молекуляр автомат"ы тип аталған был иҫ китмәле органоид.
1950-се йылдар башында, аҡһым беренсе тапҡыр яһалма рәүештә синтезлана. Был — полипептид сынйыры бары тик 51 аминокислота ҡалдығынан торған инсулин була. Уны синтезлау өсөн 5000 операция үткәрергә тура килә.
Был эште 10 кеше өс йыл буйы саҡ башҡарып сыға. Шулай итеп, лаборатория шарттарында аҡһымды синтезлау ифрат ҙур көс, ваҡыт һәм күп сығымдар талап итә.
Ә тере күҙәнәктә 200—300 аминокислоталы быуындан торған аҡһымдың бер молекулаһын синтезлау бик тиҙ— 1—2 минут эсендә башҡарыла.
Аҡһым биосинтезында ферменттарҙың роле
[үҙгәртергә | сығанаҡты үҙгәртеү]Аҡһымды синтезлау ферменттарҙың ҡатнашлығынан башҡа үтмәй. Аҡһым синтезының бөтә реакциялары ла махсус ферменттар менән катализлана. ДНК һәм и-РНК-ның синтезы ферменттар ҡатнашлығында бара.
Аминокислоталарҙың үҙҙәренең т-РНК-лары менән эләктерелеп алыныуын һәм ҡушылыуын тәьмин итеүсе айырым ферменттар бар.
Рибосомаларҙа аҡһымды йыйыу процесында аминокислоталарҙы бер-береһенә эләктерә торған фермент эшләй.
Аҡһым биосинтезы энергияһы
[үҙгәртергә | сығанаҡты үҙгәртеү]Синтездың һәр процесы энергия тотоноуҙарға мохтаж. Аҡһым биосинтезы синтетик реакциялар сынйырынан тора:
- и-РНК синтезы;
- аминокислоталарҙың т-РНК менән ҡушылыуы;
- «аҡһымды йыйыу».
Был реакцияларҙың бөтәһе лә энергия тотоноуҙарын талап итә. Аҡһым синтезы өсөн кәрәк булған энергия АТФ тарҡалған ваҡытта бүленеп сыға.
Һылтанмалар
[үҙгәртергә | сығанаҡты үҙгәртеү]- Аҡһымдар // Башҡорт энциклопедияһы. — Өфө: БР ДАҒУ «Башҡорт энциклопедияһы», 2015—2024. — ISBN 978-5-88185-143-9.
- Строение, свойства и функции белков 2017 йыл 28 декабрь архивланған.
Әҙәбиәт
[үҙгәртергә | сығанаҡты үҙгәртеү]- Лемеза Н. А., Камлюк Л. В., Лисов Н. Д. Биология в экзаменационных вопросах и ответах. (Лемеза Н. А., Комлюк А. В. Лисов Н. Д. — 10-е изд. — М.: Айрис-пресс, 2006 — 512с.: ил (Домашний репетитор)
- Чебышев Н. В., Кузнецов С. В., Зайчикова С. Г. Поступающим в ВУЗы. Биология (Чебышев Н. В. — Биология. Пособие для поступающих в ВУЗы. Том I.- М.:ООО"Издатель ОНИКС", 1999.-448с.
- Под редакцией акдемика РАМН, профессора Ярыгина В. Н. Для поступающих в ВУЗы. Биология. (А. Г. Мустафин, Ф. К. Лажуева, Н. Г. Быстренина и др., Под ред. В. Н. Ярыгина. −7-е изд., стер. _ М.: Высш.шк., 2004. — 492с. Ил.
Иҫкәрмәләр
[үҙгәртергә | сығанаҡты үҙгәртеү]- ↑ http://www.башкирская-энциклопедия.рф/index.php/read/8-statya/878-a-ymdar(недоступная ссылка)
- ↑ Ю. А. Овчинников. Биоорганическая химия. — Москва: Просвещение, 1987. — С. 24—26.
