Углерод
| |||||
| Ябай матдәнең тышҡы күренеше | |||||
|---|---|---|---|---|---|
| Атом үҙенсәлектәре | |||||
| Исеме, символы, номеры |
Углерод / Carboneum (С), 6 | ||||
| Атом массаһы (моляр массаһы) | |||||
| Электрон конфигурация |
[He] 2s2 2p2 | ||||
| Атом радиусы |
91 пм | ||||
| Химик үҙенсәлектәре | |||||
| Ковалент радиус |
77 пм | ||||
| Ион радиусы |
16 (+4e) 260 (-4e) пм | ||||
| Электроотиҫкәрелек |
2,55 (Полинг шкалаһы) | ||||
| Окисланыу дәрәжәһе |
-4, -2, 2, 4 | ||||
| Ионлашыу энергияһы (первый электрон) | |||||
| Ябай матдәнең термодинамик үҙенсәлектәре | |||||
| Тығыҙлыҡ (н. ш.) |
2,25 (графит) г/см³ | ||||
| Иреү температураһы |
3 820 K | ||||
| Ҡайнау температураһы |
5 100 K | ||||
| Моляр йылы һыйышлығы |
8,54 (графит)[1] Дж/(K·моль) | ||||
| Моляр күләм | |||||
| Ябай матдәнең кристалл рәшәткәһе | |||||
| Рәшәткә структураһы |
гексагональ (графит), кубик (алмаз) | ||||
| Рәшәткә параметры |
a=2,46; c=6,71 (графит); а=3,567 (алмаз) Å | ||||
| Отношение c/a |
2,73 (графит) | ||||
| Дебай температураһы |
1860 (алмаз) K | ||||
| Башҡа характеристикалар | |||||
| Йылы үткәреүсәнлек |
(300 K) 1,59 Вт/(м·К) | ||||
| 6 | Углерод
|
12,011 | |
| 2s22p2 | |
Углеро́д (C, лат. carboneum) — химик элемент, C хәрефе менән билдәләнә, атом һаны- 6. Элемент дүрт валентлы металл булмаған матдә, йәки ковалент химик бәйләнеш булдырыу өсөн дүрт ирекле электроны бар. Ул периодик системаның 14-се төркөмөндә (иҫкергән классификация буйына — 4-се). Был элементтың өс изотобы беҙҙең тирә-йүндә осрай. Тотороҡло (стабильный) изотоптар- 12C һәм 13C , ә 14C радиоактив изотоп (был изотоптың ярымбүленеш осоро 5730 йыл). Углерод боронғо антик донъяла уҡ билдәле булған.
Углеродтың полимер сынйыр эшләү һәләте углерод нигеҙендә берләшмәләрҙең бик ҙур класcын булдыра, улар органик берләшмәләр тип атала. Органик берләшмәләр органик булмаған берләшмәләргә ҡарағанда күберәк. Уларҙы органик булмаған химия өйрәнә.
Тарихтан
[үҙгәртергә | сығанаҡты үҙгәртеү]Ағас күмере рәүешендә углерод металдарҙы иретеү өсөн бик борондан ҡулланылған. Борондан углеродтың аллотроп модификациялары билдәле: алмас һәм графит.
XVII—XVIII быуаттар араһында Иоганн Бехер менән Георг Шталь флогестон теорияһын булдыра. Был теорияға яраҡлы һәр бер яныусан есемдә айырым элементар матдә бар, ул — ауырлыҡһыҙ флюид — яныу процесында осоп китә торған флогистон. Бик күп күмер янғандан һуң әҙ генә тороп ҡала, шуға күрә флогистиктар күмер саф флогистондан тора тип иҫәпләгән. Күмерҙең флогистлау тәьҫирен- «эзбиз» һәм тоҡомдарҙан (рудаларҙан) металлдар алыуҙы шуның менән аңлатҡандар. Һуңыраҡ йәшәгән флогистиктар (Рене Антуан Реомюр, Торберн Улаф Бергман һәм башҡалар) күмерҙең элементар матдә икәнен аңлай башлағандар."Саф күмерҙең" элементар (ябай) матдә икәнен Антуан Лавуазье тәүге булып иҫбатлай. Ул һауала һәм кислородта күмер һәм башҡа матдәләрҙең яныу процессын өйрәнә. Гитон де Морво, Лавуазье, Бертолле һәм Антуан де Фуркруаның «Химик номенклатура методы» («Метод химической номенклатуры») (1787) китабында французса «саф күмер» (charbone pur) урынына «углерод» (carbone) исеме ҡулланыла. Углерод исеме Лавуазьеның «Химиянан элементар дәреслегендәге» "Ябай есемәр таблицаһы"на ингән.
1791 йылда инглиз химигы Смитсон Теннант беренсе булып ирекле углерод алыуға ирешә; ул ҡыҙҙырылған аҡбур өҫтәнән фосфор парын ебәрә, бының һөҙөмтәһендә кальций фосфаты менән углерод барлыҡҡа килә. Алмастан ныҡ ҡыҙҙырған саҡта бер нимә лә ҡалмай икәнен әллә ҡасандан алып белгәндәр. 1751 йылда герман императоры Франц I яндырып тәжрибә үткәрер өсөн алмас менән рубин бирергә риза була, бынан һуң бындай тәжрибәләр модаға инеп китә. Яндырған саҡта алмас ҡына янып бөтә икәне билдәле була, ә ҡыҙыл яҡут- рубин (хром ҡатыш алюминий окисы) яндырыусы линзаның фокусында оҙаҡ ваҡыт йылытҡанда ла бирешмәй. Лавуазье алмасты ҙур яндырыу машинаһында яндырыу буйынса тәжрибә үткәреп ҡарай һәм алмас -кристалл углерод тигән фекергә килә. Углеродтың икенсе аллотробы — графит — алхимиктар тарафынан үҙгәргән ҡурғаш ялтырауы — свинцовый блеск тип атала һәм уны plumbago тип йөрөтәләр; 1740 йылда ғына Потт графитта бер ниндәй ҙә ҡурғаш эҙҙәрен тапмай. Шееле графитты тикшерә (1779) һәм флогистик булараҡ уны айырым төр көкөртлө есем, йәки айырым минераль күмер, «һауа кислоталы» -воздушная кислота (СО2) айырым минераль күмер һәм бик күп флогистон тип уйлай.
Егерме йылдан һуң Гитон де Морво әкрен генә йылытып, алмасты графитҡа , ә һуңыраҡ күмер кислотаһына әйләнә[2].
Исеменең килеп сығыуы
[үҙгәртергә | сығанаҡты үҙгәртеү]XVII—XIX быуаттарҙа рус химия буйынса һәм башҡа махсус китаптарҙа ҡайһы бер саҡ «углетвор» исеме ҡулланылған (Шлаттер, 1763; Шерер, 1807; Севергин, 1815); 1824 йылда Соловьёв «углерод» исемен уйлап сығара. Углерод берләшмәләренең исемендә карбо(н) — от лат. carbō (род. п. carbōnis) «уголь» һүҙе бар.
Физик сифаттары
[үҙгәртергә | сығанаҡты үҙгәртеү]Углерод бик күп төрлө физик сифатлы аллотроп модификацияларҙа бар. Модификациларҙың төрлөлөгө углеродтың төрлө химик бәйләнештәр булдыра алыуына бәйле.
Углерод изотоптары
[үҙгәртергә | сығанаҡты үҙгәртеү]Тәбиғәттә углерод ике стабиль 12С (98,93 %) һәм 13С (1,07 %) һәм бер радиоактив 14С (β-излучатель, Т½ = 5730 лет) изотобынан тора, углерод башлыса стратосфераның түбәнге өлөшөндә һәм ер ҡабығында тупланған. 14N (n, p) 14C реакцияһы буйынса азот ядроһына даими рәүештә космос нурланышы нәтижәһендә стратосфераның түбәнге ҡатламында барлыҡҡа килә. Шулай уҡ 1950-се йылдарҙан һуң атом электростанциларының һәм водород бомбаһының техноген продукты булараҡ барлыҡҡа килә.
14С 14С формалашыу һәм тарҡалыу нигеҙендә радиоуглерод менән даталау ысулы ята, был ысул геологияла һәм археологияла киң ҡулланыла.
Углеродтың аллотропные модификацияһы
[үҙгәртергә | сығанаҡты үҙгәртеү]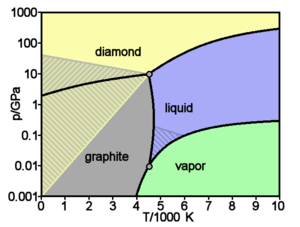
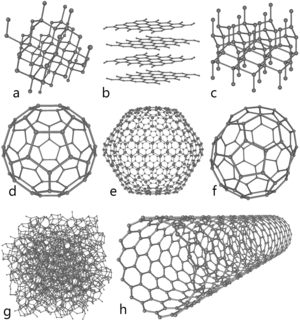
a: алмаз, b: графит, c: лонсдейлит
d: фуллерен — бакибол C60, e: фуллерен C540, f: фуллерен C70
g: аморф углерод, h: углерод нанокөпшә
Кристалл углерод
[үҙгәртергә | сығанаҡты үҙгәртеү]- Алмаз
- Графен
- Графит
- Карбин
- Лонсдейлит
- Наноалмаз
- Фуллерен
- Фуллерит
- Углерод сүс
- Углерод наносүс
- Углерод нанокөпшәләр
Аморф углерод
[үҙгәртергә | сығанаҡты үҙгәртеү]- Активлаштырылған күмер
- Ағас күмере
- Ҡаҙылма күмер: антрацит һәм ҡаҙылма күмер
- Ташкүмер коксы, нефть коксы һәм башҡалар
- Быяла угрерод
- Техник углерод
- Ҡором
- Углеродная нанокүбеге
Ғәмәлдә үрҙә һанап үтелгән аморф формалар — углеродтың таҙа аллотропик формаһы түгел, ә углерод миҡдары юғары булған химик берләшмәләр генә
Кластер формалар
[үҙгәртергә | сығанаҡты үҙгәртеү]- Астрален
- Диуглерод
- Углерод наноконусы
Ҡулланыу
[үҙгәртергә | сығанаҡты үҙгәртеү]Графит ҡәләм етештереү сәнәғәтендә ҡулланыла, әммә уның йомшаҡлығын кәметеү өсөн балсыҡ ғушалар. Шулай уҡ айырыуса юғары йәки түбән температурала майлау сараһы булараҡ ҡулланыла. Уның юғары температурала иреү нөктәһе унан металдар ҡойоу өсөн тиглдар эшләргә мөмкинлек бирә. Графиттың электр тогын үткәреү һәләте лә унан сифатлы электродтар эшләү мөмкинлеген бирә.
Алмаз үҙенең иҫ киткес ҡатылығы арҡаһында — алыштырғыһыҙ абразив материал. Алмаз япмала шымартыусы дискалар, быраулау ҡоролмалары бар. Бынан тыш, биҙәүестәрҙә ҡиммәтле бриллиант — ҡырланған алмаз. Һирәк булыуы, юғары декоратив сифаттары һәм тарихи шарттарҙы билдәләүе арҡаһында алмаз һәр ваҡыт иң ҡиммәтле таш булып тора. Алмаздың юғары термик үткәреүсәнлеге (2000 йылға тиклем W/m·K) уны ярымүткәргес технологияһы өсөн процессорҙар йәймәһе сифатында перспективалы материалға әйләндерә. Әммә алмаз сығарыуҙың сағыштырмаса юғары хаҡы (бер карат өсөн $97,47[25]) һәм алмаз эшкәртеүҙең ҡатмарлылығы уны был өлкәлә ҡулланыуҙы сикләй.
Фармакологияла һәм медицинала углеродтың төрлө берләшмәләре киң ҡулланыла: углерод кислотаһы һәм углерод кислоталары сығарылмалары, төрлө гетероциклдар, полимерҙар һәм башҡа берләшмәләр. Әйтәйек, карболен (активлаштырылған углерод), организмдан төрлө токсиндарҙы йотоу һәм сығарыу өсөн ҡулланыла; графит (май рәүешендә) — тире ауырыуҙарын дауалау өсөн; радиоактив углерод изотоптары — фәнни тикшеренеүҙәр өсөн (радиоуглерод анализы) ҡулланыла.
Кеше тормошонда углерод ҙур роль уйнай. Уның ҡушымталары был күп яҡлы элементтың үҙе кеүек төрлө. Атап әйткәндә, углерод ҡоростың (ауырлығы буйынса 2,14 % тиклем) һәм суйындың (ауырлығы буйынса 2,14 проценттан ашыу) айырылғыһыҙ өлөшө булып тора.
Углерод бөтә органик матдәләрҙең нигеҙе булып тора. Теләһә ниндәй тере организм күп осраҡта углеродтан тора. Углерод — тереклектең нигеҙе. Тере организмдар өсөн углерод сығанағы булып ғәҙәттә атмосферанан йәки һыуҙан CO2 тора. Фотосинтез һөҙөмтәһендә биологик аҙыҡ сылбырына инә, уларҙа тере йәндәр бер-береһен йәки бер-береһенең ҡалдыҡтарын ашай һәм шуның менән үҙ тәндәрен төҙөү өсөн углерод үҙләштерә. Углеродтың биологик циклы йә окисланыу һәм атмосфераға яңынан сығыу юлы менән, йә күмер, йә нефть рәүешенә инеү өсөн ерләү юлы менән тамамлана.
Ҡаҙылма яғыулыҡ рәүешендәге углерод: күмер һәм углеводородтар (нефть, тәбиғи газ) — кешелек өсөн иң мөһим энергия сығанағы.
Ағыулы тәьҫире
[үҙгәртергә | сығанаҡты үҙгәртеү]Углерод тирә-йүнгә автотранспорт эшләп сығарған газдарҙан, ТЭС-тарҙа (йылылыҡ электростанциялары) күмер яндырғанда, күмерҙе асыҡ ысул менән тапҡанда, ер аҫтында уның газға әйләнгән сағында, күмер концентраттарын яһағанда һ.б. эләгә.Янып ятҡан сығанаҡтар өҫтөндә углерод концентрацияһы 100—400 мкг/м³, ҙур ҡалалар өҫтөндә 2,4—15,9 мкг/м³, ауыл ерендә 0,5 — 0,8 мкг/м³. АЭС-тарҙың газ-аэрозоль ҡатнашмалары менән һауаға (6—15)·109 Бк/сут 14СО2 эләгә.
Углеродтың атмосфералағы аэрозолдәрҙәге дәүмәле артыу халыҡ араһында сирҙәр , бигерәк тә тын юлдары һәм үпкә сирҙәре, артыуға килтерә. Һөнәри сирҙәр — башлыса антракоз һәм туҙандан була торған бронхит. Эш зонаһындағы һауала ПДК, мг/м³ (рөхсәт ителгән конценрация): алмаз 8,0, антрацит һәм кокс 6,0, таш күмер 10,0, техник углерод һәм углерод туҙаны 4,0; атмосфера һауаһында бер тапҡыр максимум 0,15, уртаса тәүлеккә 0,05 мг/м³.
Биологик молекулалар составына ингән (айырыуса ДНК һәм РНК) 14С матдәһенең радиоактивлығы уның молекуланың химик составын үҙгәртеүсе β-киҫәксәләр (14С (β) → 14N) менән үҙ-ара радиацион тәьҫир итешеүе менән билдәләнә. 14С матдәһенең һауалағы концентрацияһы:эш зонаһында ДКА 1,3 Бк/л, атмосфера һауаһында ДКБ 4,4 Бк/л, һыуҙа 3,0·104 Бк/л, тын юлдары аша кеше организмына үтеү- 3,2·108 Бк/йылына.
Иҫкәрмәләр
[үҙгәртергә | сығанаҡты үҙгәртеү]- ↑ Редкол.:Кнунянц И. Л. (гл. ред.). Химическая энциклопедия: в 5 т. — Москва: Советская энциклопедия, 1988. — Т. 1. — С. 607. — 623 с. — 100 000 экз.
- ↑ ChemNet. Углерод: история открытия элемента.

|
Был химия буйынса тамамланмаған мәҡәлә. Һеҙ мәҡәләне төҙәтеп һәм тулыландырып проектҡа ярҙам итә алаһығыҙ. |


